Định nghĩa anken là gì? Đồng đẳng - đồng phân và danh pháp
Theo SGK Hóa học tập 11 (NXB Giáo dục đào tạo Việt Nam) đem khái niệm vô cùng rõ: “Anken là những hidrocacbon mạch hở nhưng mà nhập phân tử có một links song C=C”.
Bạn đang xem: Anken: Chi tiết lý thuyết và hướng dẫn giải bài tập trọn bộ
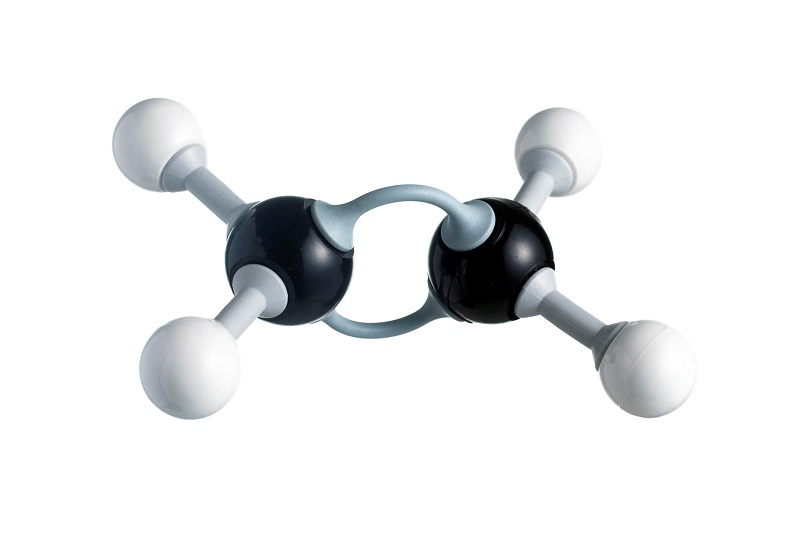
Dãy đồng đẳng anken
Etilen (CH2=CH2) và những hóa học tiếp sau đem công thức anken là C3H6, C4H8, C5H10… đem đặc điểm tương tự động etilen lập trở nên sản phẩm đồng đẳng đem công thức phân tử công cộng CnH2n (n >=2) được gọi là anken hoặc oletin.
Đồng phân
Tìm hiểu đồng phân anken tất cả chúng ta tiếp tục chuồn nhập cụ thể đồng phân cấu trúc và đồng phân hình học tập của chính nó.
- Đồng phân cấu tạo: Etilen và propilen không tồn tại đồng phân anken. Từ C4H8 trở chuồn ứng với cùng 1 công thức phân tử đem những đồng phân anken về địa điểm links song và về mạch cacbon.
- Đồng phân hình học: Trong phân tử anken, mạch đó là mạch cacbon nhiều năm nhất đem chứa chấp links song C=C. Những anken nhưng mà từng nguyên vẹn tử cacbon ở địa điểm links song liên với nhị group nguyên vẹn tử không giống nhau sẽ có được sự phân bổ không khí không giống nhau của mạch chủ yếu xung xung quanh links song. Chính sự phân bổ không giống nhau cơ đưa đến đồng phân về địa điểm không khí của những group nguyên vẹn tử gọi là đồng phân hình học tập.
Ví dụ: Với công thức cấu trúc CH3-CH=CH-CH3 đem những đồng phân hình học tập như hình bên dưới.
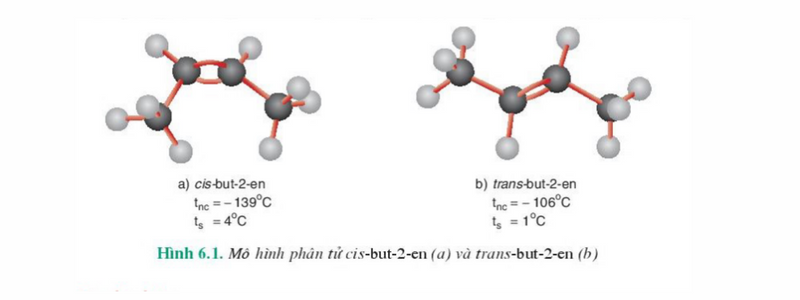
Danh pháp anken là gì?
Cách gọi thương hiệu anken bao hàm thương hiệu thường thì và thương hiệu thay cho thế.
- Cách gọi thương hiệu anken thông thường: Được gọi là thương hiệu ankan tuy nhiên thay cho đuôi “an” trở nên “ilen”. Ví dụ như etilen (C2H4), propilen (C3H6), butilen (C4H8).
- Tên thay cho thế của anken: Xuất phân phát kể từ thương hiệu ankan ứng bằng phương pháp thay đổi đuôi “an” trở nên “en”. Từ CH4 trở chuồn, nhập thương hiệu anken cần thiết thêm thắt số chỉ địa điểm nguyên vẹn tử cacbon trước tiên chứa chấp links song. Mạch cacbon được đặt số kể từ phía ngay gần links song rộng lớn.
Quy tắc được tổ hợp như sau:
-
Chọn mạch C nhiều năm nhất và đem chứa chấp links song thực hiện mạch chủ yếu.
-
Đánh số C mạch chủ yếu kể từ phía toạ lạc ngay gần links song nhất.
-
Gọi thương hiệu bám theo trật tự như sau: Số chỉ địa điểm nhánh + Tên nhánh + Tên C mạch chủ yếu + Số chỉ links song + en.
Bảng: Tên thay cho thế và một vài ba hằng số vật lý cơ của một trong những anken
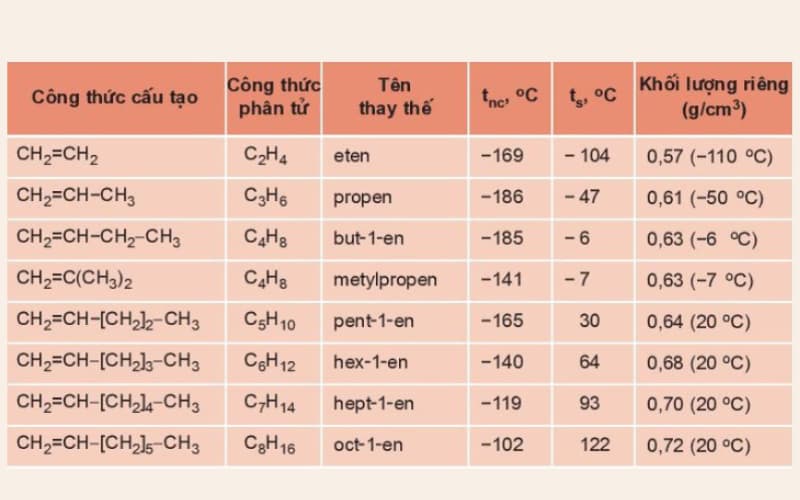
Tính hóa học vật lý cơ của anken
Nhắc cho tới đặc điểm vật lý cơ cả anken, tất cả chúng ta ko thể bỏ lỡ một vài ba đặc điểm cần thiết sau:

-
Trong ĐK thông thường, những anken kể từ C2H4 cho tới C4H8 là hóa học khí; kể từ C5H10 trở chuồn là hóa học rắn hoặc lỏng.
-
Nhiệt nhiệt độ chảy, sức nóng phỏng sôi, lượng riêng rẽ của anken tăng dần dần theo hướng tăng của phân tử khối.
-
Tất cả những anken đều nhẹ nhõm rộng lớn nước (D <1g/cm3).
-
Anken ko tan nội địa.
XÂY DỰNG NỀN TẢNG TOÁN HỌC VỮNG CHẮC CHO TRẺ TỪ NHỎ VỚI ĐA PHƯƠNG PHÁP DẠY HỌC TÍCH CỰC, CHI PHÍ CỰC RẺ CHƯA ĐẾN 2K/NGÀY CÙNG MONKEY MATH.

Tính hóa chất của anken
Liên kết song C=C bao gồm links σ và một links π (liên kết π kém cỏi bền lâu links σ) vì vậy dễ dàng và đơn giản bị phân tách rộng lớn, gây ra đặc điểm chất hóa học đặc thù của anken này đó là dễ dàng và đơn giản nhập cuộc phản xạ nằm trong tạo nên trở nên phù hợp hóa học no ứng.

Phản ứng cộng
Phản ứng nằm trong anken bao gồm phản xạ nằm trong hidro, phản xạ nằm trong halogen và phản xạ nằm trong HX.
- Phản ứng nằm trong hidro của anken: Khi đun rét đem sắt kẽm kim loại niken (hoặc platin/ plaid) thực hiện xúc tác, anken kết phù hợp với hidro tạo nên trở nên ankan ứng. Ví dụ: CH2=CH-CH3 + H2 → CH3-CH2-CH3 (Điều kiện: Ni, sức nóng độ)
- Phản ứng nằm trong halogen: Thực hiện tại thực nghiệm dẫn etilen kể từ từ chuồn nhập hỗn hợp brom, thấy gray clolor đỏ rực của hỗn hợp bị nhạt nhẽo dần dần. Ta đem phương trình như sau: CH2=CH2 + Br2 (nâu đỏ) → CH2Br-CH2Br (1,2-đibrometan, ko màu)
Tiếp tục tiến hành sụp hỗn hợp brom nhập ly đựng anken (lỏng), để ý thấy hỗn hợp brom bị thất lạc color. Ta đem phương trình phản xạ như sau: CnH2n + Br2 → CnH2nBr2

- Phản ứng nằm trong HX: Các anken cũng nhập cuộc nhập phản xạ lộn với nước, hidro halogen (HBr, HCl, HI) và với những axit mạnh. Một số ví dụ minh họa: CH2=CH2 + H-OH → CH3-CH2-OH (Điều khiếu nại H+) hoặc CH2=CH2 + H-Br → CH3-CH2-Br
Các Anken đem cấu tạo nên phân tử ko đối xứng khi tính năng với HX rất có thể sinh đi ra lếu phù hợp 2 sản phẩm. Ví dụ như:
CH3-CH=CH2 + HBr → CH3-CHBr-CH3 (2-brompropan – thành phầm chính)
CH3-CH=CH2 + HBr → CH3-CH2-CH2Br (1-brompropan – thành phầm phụ)
Quy tắc nằm trong HX hoặc còn được gọi là quy tắc Maccopnhicop (Markovnikov) sau:
-
Nguyên tử H tiếp tục gắn kèm với nguyên vẹn tử cacbon bậc thấp, ví dụ là C ở links song có không ít H rộng lớn.
-
Nhóm halide (X) tiếp tục gắn kèm với nguyên vẹn tử cacbon bậc cao, ví dụ là C ở links song đem không nhiều H rộng lớn.
-
Sản phẩm chủ yếu của phản xạ đó là thành phầm được tạo nên trở nên bám theo quy tắc Maccopnhicop.
Phản ứng trùng hợp
Ở sức nóng phỏng và áp suất cao với hóa học xúc tác tương thích, những phân tử anken rất có thể kết phù hợp với nhau tạo nên trở nên những mạch vô cùng nhiều năm và đem phân tử khối rộng lớn.
Ví dụ:
… + CH2=CH2+CH2=CH2+CH2=CH2+…→… -CH2-CH2-CH2-CH2-CH2-CH2-… (Điều kiện: Nhiệt phỏng, p, xúc tác)
Phương trình thu gọn gàng như sau:
nCH2=CH2 → (-CH2–CH2-)n (Polietylen hoặc PE)
Phản ứng trùng khớp nằm trong loại phản xạ polime hóa, là quy trình links nhiều phân tử nhỏ như thể nhau hoặc tương tự động nhau muốn tạo trở nên những phân tử rất rộng, gọi là polime. Trong đó:
-
Chất đầu (CH2 = CH2) là monome.
-
-CH2 – CH2– là vướng xích của polime.
-
n là thông số trùng khớp.
Phản ứng oxi hóa
Phản ứng lão hóa trọn vẹn và phản xạ lão hóa ko trọn vẹn cũng là một trong trong mỗi đặc điểm chất hóa học cần thiết của anken.
Phản ứng lão hóa trả toàn
Khi bị nhen nhóm với oxi, etilen và những đồng đẳng có khả năng sẽ bị cháy và lan đi ra sức nóng.
CnH2n + 3n/2 O2 → nCO2 + nH2O
Phản ứng lão hóa ko trọn vẹn của anken
Để thực hiện rõ ràng phản xạ lão hóa ko trọn vẹn của anken, tao tiến hành thực nghiệm sục khí etilen nhập hỗn hợp KMnO4. Quan sát thấy color của hỗn hợp tiếp tục nhạt nhẽo dần dần và đem kết tủa gray clolor thâm của MnO2.
Ta đem phản xạ như sau:
3CH2=CH2 + 4H2O + 2KMnO4 → 3HO-CH2-CH2-OH + 2MNO4 (kết tủa) + 2KOH
Xem thêm:
- Ankin là gì? Lý thuyết và giải bài bác tập luyện chi tiết
- Muối amoni: Chi tiết lý thuyết và bài bác tập luyện kèm cặp tiếng giải
- Axit photphoric (H3PO4) là gì? Cấu tạo nên phân tử, đặc điểm, phần mềm và cách thức điều chế
Điều chế anken như vậy nào?
Cách pha trộn anken nhập chống thực nghiệm và tạo ra nhập công nghiệp đem sự khác lạ.
Cách pha trộn anken nhập chống thí nghiệm
Trong chống thực nghiệm, etilen được pha trộn kể từ ancol etylen
C2H5OH → CH2=CH2 + H2O (Điều kiện: H2SO4 quánh, 170 phỏng C)
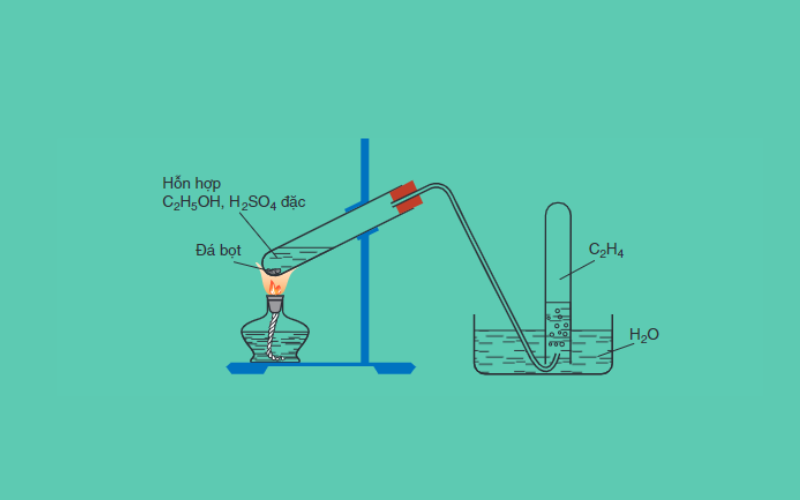
Cách pha trộn Anken nhập công nghiệp
Trong công nghiệp, anken được pha trộn kể từ ankan:
CnH2n+2 → CnH2n + H2 (Điều kiện: Nhiệt phỏng, p, xúc tác)
Các anken và dẫn xuất của anken là vật liệu mang đến quy trình tạo ra chất hóa học. Một số phần mềm cần thiết của anken là:
-
Sử dụng nhập sản xuất màng mỏng manh, ống dẫn nước, bình chứa… bằng phương pháp trùng khớp etilen, propilen, butilen… nhận được polime.
-
Anken cũng khá được phần mềm nhập tạo ra rượu, dẫn xuất halogen hoặc một trong những hóa học không giống.
-
Monome được gửi hóa kể từ Etilen nhằm tổ hợp một loạt polime đáp ứng nhu cầu yêu cầu đa dạng của cuộc sống, nghệ thuật.
Phân biệt anken và ankan
Để phân biệt anken và ankan, tao dùng hỗn hợp brom. Khi sụp brom nhập ly đựng anken (lỏng) tiếp tục thấy hỗn hợp brom bị thất lạc color trong những lúc cơ ankan thì ko làm mất đi color hỗn hợp brom.
Ngoài brom, tất cả chúng ta cũng rất có thể sử dụng dung dịch tím (KMnO4) nhằm nhận ra anken. Anken làm mất đi color hỗn hợp dung dịch tím nên dễ dàng dạng nhằm nhận ra.
Bài tập luyện về anken SGK Hóa học tập 11 kèm cặp tiếng giải chi tiết
Sau khi vẫn lần hiểu những kỹ năng lý thuyết về anken, chúng ta hãy tích vô cùng thực hiện thêm thắt những bài bác tập luyện nhập SGK nhằm ôn tập luyện và áp dụng ngay lập tức những gì một vừa hai phải lần nắm được.
Xem thêm: Những thể loại rác phẩm mà tôi ghét - [Ngoài lề] Trace tranh

Bài tập luyện 2 (SGK Hóa học tập 11, trang 132)
Ứng với công thức C5H10 đem từng nào đồng phân cấu trúc ?
A. 4; B. 5 ; C. 3 ; D. 7
Gợi ý đáp án:
Đáp án thực sự B. 5
Các công thức cấu tạo:
Bài tập luyện 3 (SGK Hóa học tập 11, trang 132)
Viết phương trình chất hóa học của phản xạ xẩy ra khi:
a. Propilen tính năng với hidro, đun rét (xúc tác Ni).
b. But-2-en tính năng với hidro clorua.
c. Metylpropen tính năng với nước đem xúc tác axit.
d. Trùng phù hợp but-1-en.
Gợi ý đáp án:
Bài tập luyện 4 (SGK Hóa học tập 11, trang 132)
Trình bày cách thức chất hóa học để:
a. Phân biệt metan và etilen.
b. Tách lấy khí metan kể từ lếu phù hợp etilen.
c. Phân biệt nhị bình ko dán nhãn đựng hexan và hex-1-en.
Viết phương trình hoá học tập của phản xạ vẫn sử dụng.
Gợi ý đáp án:
a. Lần lượt mang đến metan và etilen trải qua hỗn hợp nước brom, hóa học này thực hiện hỗn hợp nước brom nhạt nhẽo color thì này đó là etilen, hóa học này ko thực hiện hỗn hợp nước brom nhạt nhẽo color thì này đó là metan.
CH2=CH2 + Br2 → CH2Br-CH2Br
Br2(dd nâu đỏ); CH2Br-CH2Br (không màu)
CH4 ko tính năng với hỗn hợp nước brom
b. Cho lếu phù hợp khí (CH4 và C2H4) trải qua hỗn hợp nước brom dư, C2H4 tiếp tục tính năng với hỗn hợp nước brom, khí sót lại thoát ra khỏi bình hỗn hợp nước brom là CH4.(PTHH như câu a)
c. Tương tự động câu a
Lần lượt mang đến hexan và hex-1-en trải qua hỗn hợp nước brom, hóa học này thực hiện hỗn hợp nước brom nhạt nhẽo color thì này đó là hex-1-en, hóa học này ko thực hiện hỗn hợp nước brom nhạt nhẽo color thì này đó là hexan
PTHH:
CH2=CH-[CH2]3-CH3 + Br2 → CH2Br-CHBr-[CH2]3-CH3
Br2(dd nâu đỏ); CH2Br-CHBr-[CH2]3-CH3 (không màu)
Hexan ko tính năng với hỗn hợp nước brom
Bài tập luyện 5 (SGK Hóa học tập 11, trang 132)
Chất này tại đây làm mất đi color hỗn hợp brom?
A. Butan
B. but-1-en
C. cacbon đioxi
D. metylpropan
Gợi ý đáp án:
Đáp án thực sự B
PTHH:
CH2=CH-CH2-CH3 + Br2 → CH2Br-CHBr-CH2-CH3
Br2(dd nâu đỏ); CH2Br-CHBr-CH2-CH3(không màu)
Bài tập luyện 6 (SGK Hóa học tập 11, trang 132)
Dẫn kể từ từ 3,36 lít lếu phù hợp bao gồm etilen và propilen (đktc) nhập hỗn hợp brom thấy hỗn hợp bị nhạt nhẽo color và không tồn tại khí bay đi ra. Khối lượng hỗn hợp sau phản xạ tăng 4,90gam.
a. Viết những phương trình chất hóa học và phân tích và lý giải những hiện tượng lạ ở thực nghiệm bên trên.
b. Tính bộ phận Phần Trăm về thể tích của từng khí nhập lếu phù hợp thuở đầu.
Gợi ý đáp án:
a. Phương trình hóa học:
CH2=CH2 + Br2 (dd, nâu đỏ) → CH2Br-CH2Br (không màu)
CH2=CH-CH3 + Br2 (dd, nâu đỏ) → CH2Br-CHBr-CH3 (không màu)
b. Gọi số mol của etilen và propilen theo thứ tự là x và hắn mol.
Khối lượng hỗn hợp sau phản xạ tạo thêm đó là lượng của lếu phù hợp etilen và propilen.
Ta có:
N(hh) = x+ hắn = 3,36/22.4 = 0.15.
M (hh) = 28x = 42y = 4.9
Giải hệ phương trình tao được x = 0.1 mol và hắn = 0.05 mol.
%VC2H4 = nC2H4 = (0.1/0.15) x 100% = 66.67%.
% VC3H6 = 100% - 66,67% = 33.33%.
Bài tập luyện về Anken - Hóa học tập 11 nhằm những em tự động luyện
Ngoài bài bác tập luyện Anken nhập SGK, bên dưới đấy là một trong những bài bác tập luyện không giống nhằm những em tự động luyện:
Bài 1: 2,8 gam anken X làm mất đi color một vừa hai phải đầy đủ hỗn hợp chứa chấp 8 gam Br2. Hiđrat hóa X chỉ nhận được một ancol có một không hai. X mang tên là gì?
Bài 2: Hỗn phù hợp khí X bao gồm H2 và C2H4 có tỉ khối đối với He là 3,75. Dẫn X qua quýt Ni nung rét, nhận được lếu phù hợp khí Y đem tỉ khối đối với He là 5. Tính hiệu suất của phản xạ hiđro hoá?
Bài 3: Dẫn 3,36 lít lếu phù hợp X bao gồm 2 anken là đồng đẳng tiếp đến vào trong bình nước brom dư, thấy lượng bình gia tăng 7,7 gam. Tìm CTPT của 2 anken?
Bài 4: Dẫn kể từ từ 6,72 lit (đktc) lếu phù hợp X bao gồm etilen và propilen và hỗn hợp brom, hỗn hợp brom bị nhạt nhẽo color, và không tồn tại khí bay đi ra. Khối lượng hỗn hợp sau phản xạ tăng 9,8 gam. Thành phần Phần Trăm bám theo thể tích của etilen nhập X là bao nhiêu?
Bài 5: Dẫn 3,36 lít (đktc) lếu phù hợp X bao gồm 2 anken là đồng đẳng tiếp đến vào trong bình nước brom dư, thấy lượng bình gia tăng 7,7 gam. Thành phần phần % về thể tích của nhị anken là bao nhiêu?
Bài 6: Cho hiđrocacbon X phản xạ với brom (trong dung dịch) bám theo tỉ lệ thành phần mol 1 : 1, nhận được hóa học cơ học Y (chứa 74,08% Br về khối lượng). Khi X phản xạ với HBr thì nhận được nhị thành phầm cơ học đem cấu trúc không giống nhau. Tên gọi của X là gì?
Bài 7: Cho H2 và 1 olefin rất có thể tích đều bằng nhau qua quýt niken đun rét tao được lếu phù hợp A. tường tỉ khối khá của A đối với H2 là 23,2. Hiệu suất phản xạ hiđro hoá là 75%. Công thức phân tử olefin là gì?
Bài 8: Cho hiđrocacbon X phản xạ với brom (trong dung dịch) bám theo tỷ trọng mol 1: 1 thì được hóa học cơ học Y (chứa 74,08% brom về khối lượng). Khi X phản xạ với HBr thì nhận được nhị thành phầm cơ học đem cấu trúc không giống nhau. Tên gọi của X là gì?
Xem thêm: VietnamAirlines | Đặt vé máy bay Vietnam Airlines Khuyến Mãi
Bài 9: Trộn 1 mol anken X với một,6 mol H2 rồi dẫn lếu phù hợp qua quýt Ni nung rét nhận được lếu phù hợp Y. Dẫn lếu phù hợp Y nhập brom dư thấy đem 0,2 mol Br2 đã phản xạ. Hiệu suất phản xạ hiđro hóa là gì?
Bài 10: Hỗn phù hợp X bao gồm H2, C2H4, C3H6 đem tỉ khối đối với H2 là 9,25. Cho 22,4 lit X (dktc) vào trong bình đựng kín đã có sẵn trước không nhiều bột Ni. Đun rét bình một thời hạn nhận được lếu phù hợp khí Y đem tỉ khối đối với H2 vì chưng 10. Tổng số mol H2 vẫn phản xạ là bao nhiêu?
Hy vọng những vấn đề share nhập nội dung bài viết bên trên vẫn khiến cho bạn gọi hiểu rộng lớn về anken và vận dụng chất lượng nhập quy trình tiếp thu kiến thức bên trên lớp. Theo dõi trang web của Monkey thông thường xuyên nhằm update những nội dung bài viết share kỹ năng môn Hóa, Vật lý và Toán cùng với rất nhiều chủ thể không giống nữa đấy.